暨南大学最新Cell子刊:靶向IL-17C,治疗子宫内膜异位症相关卵巢癌
来源:生物世界 2025-11-25 09:38
该研究揭示了 IL-17C 信号是子宫内膜异位症癌变的驱动因素,并提出了 IL-17C/IL-17RE 可作为子宫内膜异位症相关卵巢癌(EAOC)的有前景的治疗新靶点。
卵巢癌(Ovarian cancer)是全球最致命的妇科恶性肿瘤。这种癌症相对罕见,但在患有子宫内膜异位症(Endometriosis)的女性中更为常见,尤其是透明细胞卵巢癌。
子宫内膜异位症相关卵巢癌(EAOC)在子宫内膜异位症患者中的发生率高达 4.5%,其主要由卵巢病变(子宫内膜异位囊肿)恶变所致。在过去的几十年里,子宫内膜异位症的发病率有所上升,与此同时,在子宫内膜异位症患者中卵巢肿瘤的检出率也有所增加。与其它卵巢癌相比,EAOC 存在一些尚未解决的问题,包括化疗耐药性、预后较差以及发病年龄更小。
然而,子宫内膜异位症与卵巢癌之间的因果关系仍有待确定。因此,阐明这种恶性肿瘤的发病机制对于防止诊断延误以及降低其长期发病率至关重要。
2025 年 11 月 20 日,暨南大学医学院李平、香港中文大学(深圳)第二附属医院王明华、暨南大学附属第一医院周宏等人,在 Cell 子刊 Cell Reports Medicine 上发表了题为:Therapeutic targeting of interleukin-17C signaling in carcinogenesis of endometriosis 的研究论文。
该研究揭示了 IL-17C 信号是子宫内膜异位症癌变的驱动因素,并提出了 IL-17C/IL-17RE 可作为子宫内膜异位症相关卵巢癌(EAOC)的有前景的治疗新靶点。

子宫内膜异位症相关卵巢癌(EAOC)主要由子宫内膜异位囊肿恶变而来,但其机制尚不完全明确。
在这项最新研究中,研究团队对正常子宫内膜、子宫内膜异位囊肿(也被称为巧克力囊肿)和 EAOC 人类样本的空间转录组分析发现,白细胞介素-17C(IL-17C)信号通路被激活,且 EAOC 中白细胞介素-17 受体 E(IL-17RE)的表达更高。此外,患有卵巢癌的女性腹腔液中 IL-17C 浓度显著升高。
在过表达 IL-17RE 的子宫内膜异位症小鼠模型中,腹腔液中 IL-17C 水平升高。此外,IL-17C 基因敲除降低了腹腔液中 IL-17C 浓度,并抑制了子宫内膜异位症小鼠异位病灶的生长。另外,研究团队通过阻断和调控人子宫内膜异位上皮细胞、子宫内膜类器官和卵巢子宫内膜异位症小鼠的 IL-17C/IL-17RE 通路,进一步揭示了 IL-17C 信号在促进子宫内膜异位症癌变中的作用。
该研究的亮点:
子宫内膜异位症癌变的空间转录组学分析;
在卵巢癌患者腹腔液中发现 IL-17C 水平升高;
子宫内膜异位症细胞在癌变过程中 IL-17RE 表达升高;
IL-17C 基因敲除通过降低 IL-17C 水平抑制子宫内膜异位症生长。
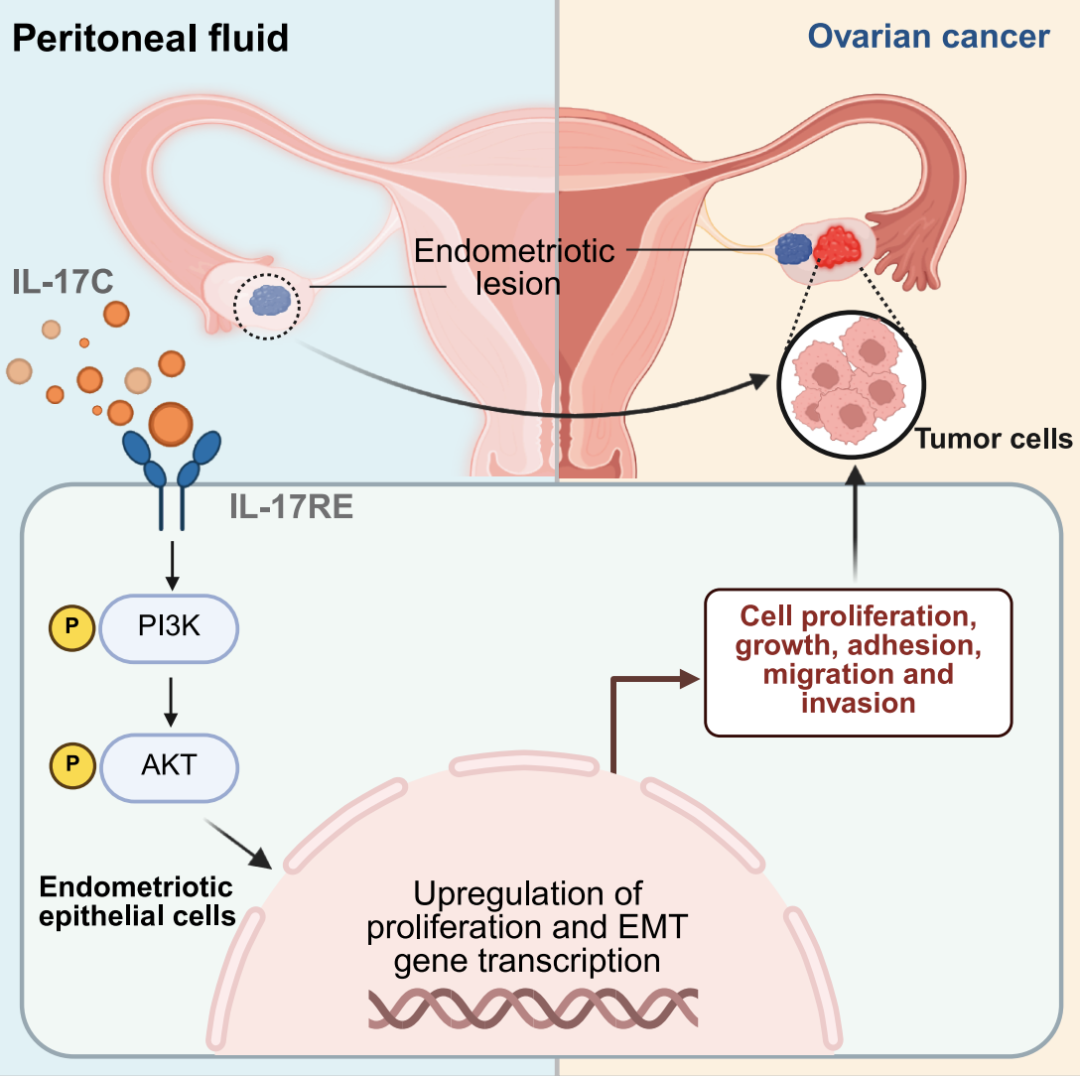
总的来说,这项研究表明,IL-17C 信号转导是子宫内膜异位症癌变的驱动因素,并提出 IL-17C/IL-17RE 作为有前景的治疗靶点,尤其是对于高表达 IL-17C 的子宫内膜异位症相关卵巢癌(EAOC)。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


